 |
| Atom dan Partikel Penyusunnya |
Atom dan Partikel Penyusunnya
1. Partikel Sub Atom
Perhatikan materi di sekeliling kita, baik yang berupa zat tunggal maupun campuran, terdiri atas butir-butir kecil atau partikel. Zat tunggal terdiri atas sejenis partikel, sedangkan campuran terdiri atas dua atau lebih jenis partikel yang tercampur begitu saja tanpa reaksi kimia. Partikel materi dapat berupa atom, molekul, atau ion. Partikel materi tersebut mempunyai ukuran sangat kecil, sehingga hampir mustahil untuk mengamatinya.
Namun, berkat kemajuan sains dan teknologi, saat ini telah berhasil ditemukan partikel paling kecil yang disebut quark atau dalam bahasa Indonesia disebut sebagai kuark. Anggapan bahwa atom merupakan bola kecil yang kompak dan tidak dapat dipecahkan lagi menjadi partikel yang lebih sederhana ternyata tidak benar. Penemuan keradioaktifan oleh Antonie Henri Becquerel ratusan tahun yang lalu telah membuktikan bahwa atom tersusun atas partikel-partikel yang lebih kecil lagi, yaitu elektron (ditemukan oleh Joseph John Thomson), proton (ditemukan oleh Ernest Rutherford), dan neutron (ditemukan oleh James Chadwick).
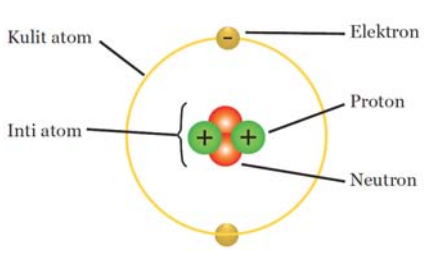
Satu atom, menurut ilmu kimia, terstruktur atas inti atom yang terdiri atas proton (bermuatan positif) dan neutron (netral), serta elektron yang bermuatan negatif dan beredar mengelilingi inti dalam lintasan-lintasan tertentu yang disebut kulit atom dan orbital atom. Jumlah proton = jumlah elektron (karena atom bersifat netral) menunjukkan nomor atom. Jumlah proton atau elektron + neutron menunjukkan bobot atom.
Pada atom netral, jumlah proton dan jumlah elektron sama banyaknya. Masing-masing partikel penyusun subatom tersebut mempunyai massa. Elektron mempunyai massa sangat kecil dibandingkan dengan massa proton dan neutron. Oleh sebab itu massa atom akan terpusat pada inti atom saja.
Pada bagian sebelumnya kamu telah mengetahui bahwa molekul air tersusun atas dua atom hidrogen (H) dan satu atom oksigen (O). Tahukah kamu, walaupun atom merupakan unit terkecil penyusun molekul, materi yang sudah sangat kecil ini ternyata tersusun dari bagian yang lebih kecil lagi yang disebut partikel subatom.
 |
| Bagian dari Atom |
Bagaimana kita tahu bahwa atom tersusun atas partikel-partikel subatom?
Amati warna lampu-lampu neon pada Gambar 6 dibawah ini. Masing-masing lampu tersebut berisi gas mulia berturut-turut helium (He), neon (Ne), argon (Ar), kripton (Kr), dan xenon (Xe)
 |
| Lampu berisi gas mulia He, Ne, Ar, Kr dan Xe |
Lampu-lampu tersebut mengeluarkan cahaya berwarna-warni setelah dialiri arus listrik. Gas-gas yang dilewati oleh aliran listrik tersebut berpendar sehingga menghasilkan cahaya berwarna-warni. Cahaya itu disebabkan oleh loncatan elektron-elektron yang menyusun atom-atom gas.
Contoh lain adalah kembang api. Apakah kamu melihat cahaya berwarna-warni dari kembang api ketika dibakar? Mengapa cahaya yang muncul berwarna-warni? Jika cahaya lampu disebabkan oleh aliran listrik, maka pada kembang api cahaya itu dihasilkan dari terbakarnya unsur-unsur yang ada dalam kembang api tersebut. Akibat temperatur yang tinggi, elektron-elektron dari atom-atom penyusun unsur itu akan berpindah dari kulit atom yang lebih tinggi ke kulit atom yang lebih rendah.
Tahukah kamu apa itu elektron?
Elektron adalah partikel subatom yang bermuatan negatif dan umumnya ditulis sebagai e¯. Para ilmuwan telah mempelajari atom sejak ratusan tahun lalu. Para ilmuwan tersebut mengemukakan teori-teori tentang atom. Teori yang satu akan runtuh atau ditolak ketika ada data atau fakta baru yang ditemukan tentang atom sehingga melahirkan teori atom yang baru. Berikut ini merupakan perkembangan teori atom:


Teori atom yang paling terkini adalah teori atom mekanika gelombang. Teori ini akan kamu pelajari ketika kamu duduk di Sekolah Menengah Atas.
Berdasarkan teori atom Bohr, dapatkah kamu menjelaskan bagaimana lampu yang yang berisi gas mulia dapat menghasilkan cahaya yang berwarna-warni? Begitu juga bagaimana terbentuknya cahaya warna-warni dari kembang api?
Menurut Bohr, atom mempunyai kulit-kulit atom tempat elektron mengelilingi inti atom. Kulit atom yang paling dekat dengan inti atom mempunyai energi paling rendah. Kulit atom yang lebih di luar mempunyai energi lebih tinggi. Elektron yang berada pada kulit atom paling dalam dapat berpindah ke kulit atom yang lebih luar bila menyerap energi dari luar atom. Energi itu dapat berasal dari panas pembakaran atau dari energi listrik yang melewati atom-atom itu.
Elektron yang terletak pada kulit atom paling luar akan mendapatkan gaya tarik yang lemah dari inti atom. Oleh karena itu elektron pada kulit atom paling luar mudah lepas dari kulit itu, sehingga atom dapat kehilangan elektron. Bila jumlah elektron dan jumlah proton dalam suatu atom tidak sama maka atom tersebut akan bermuatan atau menjadi ion. Proses pembentukan ion disebut ionisasi. Tahukah kamu, elektron-elektron yang ada pada kulit atom paling luar mempunyai peranan yang sangat penting pada pembentukan ikatan kimia antar atom dalam suatu molekul?
2. Nomor Atom dan Nomor Massa
Masih ingatkah kamu dengan materi tentang unsur? Unsur merupakan zat tunggal (murni) yang tidak dapat diubah lagi menjadi bahan lain dengan reaksi kimiawi, seperti emas, besi, perak, oksigen, dan masih banyak yang lain. Saat ini ada sekitar 105 unsur yang ditemukan di alam. Masing-masing unsur tersebut memiliki karakteristik yang berbeda-beda.
Atom-atom dari unsur yang berbeda memiliki jumlah partikel subatom yang berbeda. Semua atom dalam suatu unsur tertentu memiliki jumlah proton yang sama di dalam intinya. Jumlah proton ini unik untuk setiap unsur. Nomor massa suatu atom ditentukan oleh jumlah dari neutron, proton, dan elektron. Namun, karena massa elektron sangat kecil, maka dapat diabaikan. Atom yang satu berbeda dengan atom yang lain karena mempunyai elektron, proton, dan neutron yang berbeda jumlahnya. Jika massa atomnya berbeda maka jari-jari bola atom itu akan berbeda pula. Hubungan nomor atom, nomor massa, dan jumlah neutron dalam suatu atom yang netral (tidak bermuatan) dapat dituliskan dengan persamaan berikut.
Nomor atom = Jumlah proton (p) dalam suatu atom = jumlah elektron (e)
Nomor massa = Jumlah proton (p) + Jumlah neutron (n)
Pada penulisan lambang unsur, nomor atom ditulis subscrip (turun) di kiri lambang unsur, sedangkan nomor massa ditulis superscrip (naik) di kiri atas lambang unsur, sebagaimana berikut.

Sebagai contoh, penulisan lambang unsur litium (Li) yang mempunyai nomor atom 3 dan nomor massa 7 adalah 3/7 Li. Agar kamu dapat lebih memahami penulisan lambang atom, menentukan nomor massa, jumlah proton, serta jumlah elektronnya, coba lengkapi tabel berikut! Gunakan contoh di atas untuk menentukan jumlah proton, neutron, elektron, dan nomor massa suatu atom!
 |
| Lengkapi Kolom yang Kosong |
Keterangan:
e = elektron, p = proton, n = neutron, Z = nomor atom, A = nomor massa
Beberapa unsur seperti emas (Au), perak (Ag), dan platina (Pt) merupakan unsur-unsur logam mulia yang mempunyai nilai ekonomi tinggi. Sebagian besar unsur yang ada di alam sangat penting untuk kehidupan. Namun, beberapa unsur seperti merkuri (20080Hg), timbal (20982 Pb), dan logam berat lain, merupakan unsur yang berbahaya bagi tubuh makhluk hidup terutama manusia. Unsur ini tidak dapat didaur ulang dalam tubuh dan sulit untuk dikeluarkan, karena dalam tubuh kita tidak ada mekanisme yang berfungsi untuk menghilangkan unsur ini. Logam berat ini mampu bertahan dalam tubuh sepanjang hayat kita. Konsentrasi dari logam berat ini dapat bertambah sepanjang waktu atau dikenal dengan bioakumulasi. Logam berat ini dapat menyebabkan berbagai penyakit seperti kanker dan bahkan dapat menyebabkan kematian. Seorang wanita yang hamil juga dapat mengalami keguguran dan melahirkan bayi yang cacat akibat kandungan logam berat dalam tubuhnya.
Pernahkah kamu mendengar penyakit Minamata?
Penyakit ini pertama kali diidentifikasi pada tahun 1956 di teluk Minamata, Jepang. Di teluk Minamata ini terdapat pelabuhan ikan dan pabrik pupuk dan senyawa kimia lain yang dalam prosesnya menggunakan merkuri (Hg). Suatu ketika merkuri ini bocor dan masuk kedalam lautan serta mengkontaminasi ikan dan hewan laut lainnya. Masyarakat sekitar yang mengkonsumsi ikan yang terkontaminasi merkuri mengalami bioakumulasi merkuri dalam tubuhnya. Bioakumulasi merkuri ini menyebabkan keterbelakangan mental, cacat lahir, buta dan tuli, serta menyebabkan kematian. Kejadian ini membuat perhatian warga dunia untuk lebih menjaga dan melindungi lingkungan dari pencemaran, khususnya logam berat.
